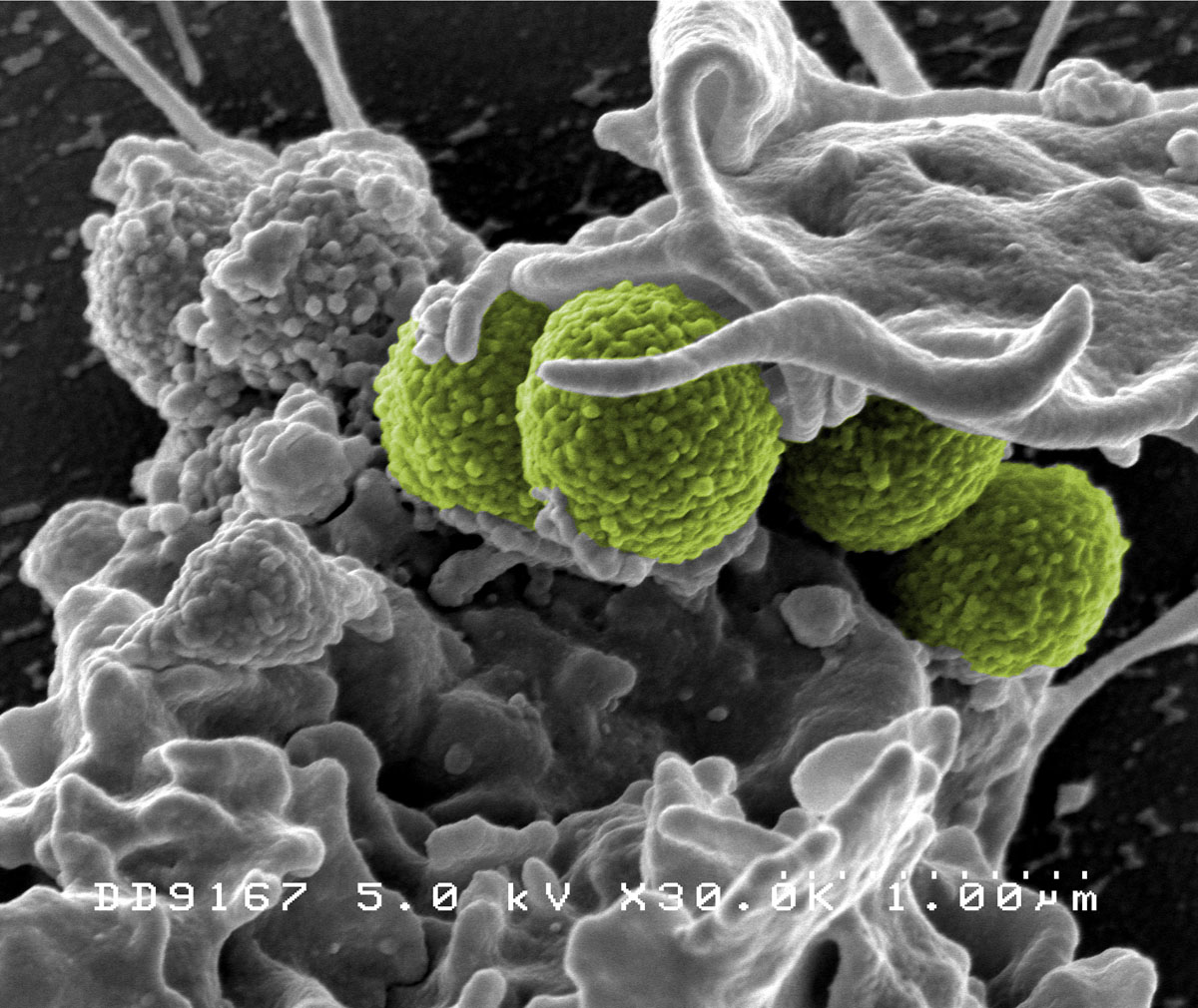
Los fragmentos de ADN que hacen que las bacterias sean peligrosas pueden ser captados y usados para eliminar a los microbios.
Los tramos de ADN llamados islas de patogenicidad pueden saltar entre cepas de bacterias, introduciendo nuevos genes productores de toxinas que generalmente hacen que una cepa sea más dañina.
Los científicos ahora han modificado las islas de patogenicidad al reemplazar los genes productores de toxinas con genes que inutilizan o matan a la bacteria Staphylococcus aureus.
Si el enfoque funciona con los humanos, podría ofrecer una alternativa a los antibióticos tradicionales que algún día podrían ser inútiles contra las cepas mortales resistentes al fármaco Staphylococcus.
Las islas de patogenicidad ya están preparadas para tales trabajos internos: Los tramos del ADN se agrupan de forma natural en pequeños paquetes que pueden ingresar fácilmente a las bacterias para generar nuevos genes. Los investigadores convirtieron esas instlas en caballos de Troya, reemplazando los genes productores de toxinas con secuencias de la herramienta de edición de genes CRISPR / Cas9, que corta el ADN en lugares específicos.
En una versión, el Cas9 corta el ADN del estafilococo, matando a las bacterias. En otra, una versión modificada de CRISPR / Cas9 no hace ningún corte y en cambio, el Cas9 se aferra a un gen que controla cuán peligrosas son las bacterias estafilocócicas para que sean menos efectivas en causar infecciones.
Los investigadores probaron en ratones estos paquetes cargados de ADN, a los que se refieren como “drones”. Ambas versiones, cuando se inyectaron bajo la piel de los ratones, impidieron que los animales desarrollaran un absceso. Y los ratones que recibieron la versión para matar bacterias sobrevivieron una inyección letal de S. aureus.
El tratamiento con drones es algo parecido a la terapia con fagos, una alternativa a los antibióticos donde los pacientes reciben un cóctel de diferentes bacteriófagos, virus que atacan a las bacterias.
La terapia con fagos, a menudo utilizada contra infecciones resistentes a múltiples fármacos, actualmente no está aprobada para su uso en los Estados Unidos, pero es común en Europa del Este.
El enfoque de los drones es más simple, dice el coautor Richard Novick, microbiólogo de la Escuela de Medicina de la Universidad de Nueva York. Para que un fago mate una célula, necesita reproducirse dentro de la célula. Pero con un “dron”, todo lo que tiene que hacer es expresar un gen, y eso matará a las bacterias.
Sin embargo, la resistencia todavía podría ser un problema con el nuevo enfoque. Algunas cepas de bacterias no reaccionaron a ninguna de las versiones del tratamiento en ratones.
Si el enfoque se usa clínicamente, y eso aún está muy lejos, un paciente probablemente recibirá múltiples tipos de drones que atacan a bacterias de diferentes maneras.
Un próximo paso es probar el sistema en otras infecciones que pueden ser causadas por estafilococos, como la neumonía.
Más información: Nature